우리 주변에 존재하는 다양한 물질들을 크게 나누면 ‘극성(polar)’물질과 ‘무극성(nonpolar)’ 물질로 나눌 수 있습니다.
가장 대표적인 물질로는 물이 있으며, 무극성 물질로는 기름이 있습니다.
일반적으로 극성 물질은 극성 물질과 서로 섞이고 무극성 물질은 무극성 물질과 서로 잘 섞이게 되어 있습니다.
이러한 이류는 서로 작용하는 힘의 크기가 비슷하기 때문입니다.
극성 물질이란 물질을 이루는 원자들이 배열을 할 때 서로 대칭을 이루지 못하여 전하의 치우침이 발생하여
부분적인 ( + )와 ( - )를 가지고 있는 물질을 말하는 것입니다.
이렇게 부분적인 ( + )와 ( - )를 가지게 되면 비슷한 성질을 가진 물질들을 잘 녹이게 됩니다.

무극성 물질이란 물질을 이루는 원자들이 배열을 할 때 서로 대칭을 이루어 극성을 가지지 않는 물질을 말하는 것입니다.
극성을 가지지 않기 때문에 자신과 비슷한 성질을 가지고 있는 물질과 섞이게 되는 것입니다.

이렇게 다른 성질을 가지고 있는 극성 물질과 무극성 물질을 서로 섞어 놓는다면 어떨까요?
그러면 두 가지 물질은 서로 섞이지 않고 층을 이루게 됩니다.
이렇게 극성 물질은 무극성 물질과 서로 다른 성질을 가지고 있습니다.
* 실험 준비물
증류수(H2O), 다이클로로 메테인(dichloromethane, CH2Cl2), 스포이트, 핀셋, 바이알 병(유리병), 포스트잇, 색연필, 네임펜

* 실험 주의사항
디클로로메테인은 휘발성이 크고 특유의 냄새가 나는 용액입니다. 섭취, 흡입 시 유독해 마시거나 냄새를 맡지 마세요. 피부에 따끔거리는 자극을 일으키므로 피부에 묻지 않도록 주의하세요. 피부에 묻었을 때 흐르는 물에 충분히 씻어주세요.
* 실험 방법
1. 깨끗한 바이알병에 디클로로 메테인을 반 정도 채운다.
2. 네임펜을 다이클로로메테인에 넣어 색을 입힌다.
3. 용액이 든 디바이알 병을 증류수로 가득 채운다.



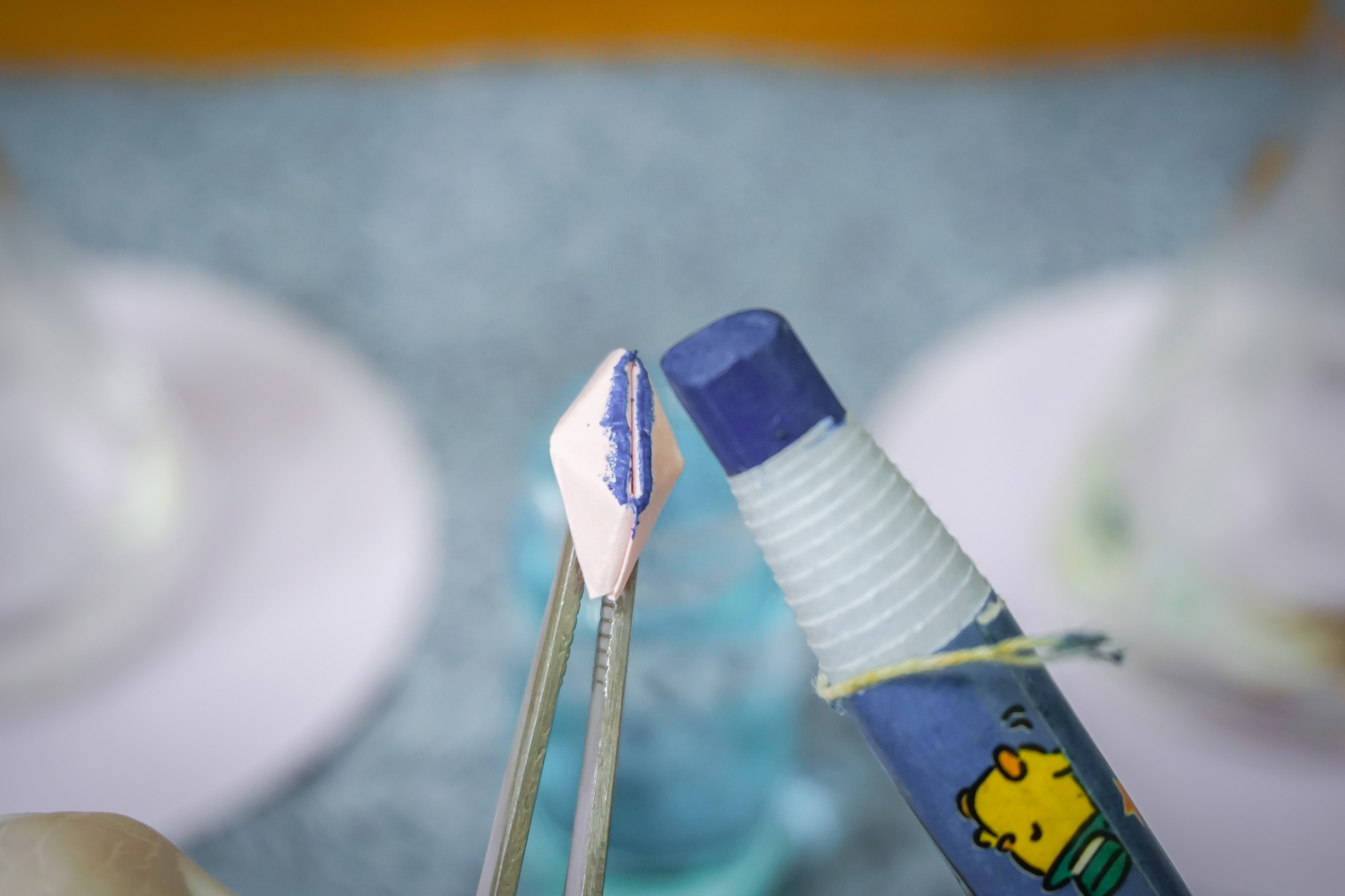
4.종이배 바닥면을 색연필로 색칠한다.
5.만들어진 종이배를 핀셋으로 잡고 두 용액의 경계면에 가져간다.
6. 종이배가 안정적으로 뜨는지 관찰해본다.



7. 뚜껑을 닫고 이리저리 흔들어 보면 물과 다이클로로메테인 경계면 사이에서만 떠있는 걸 관찰할 수 있어요.


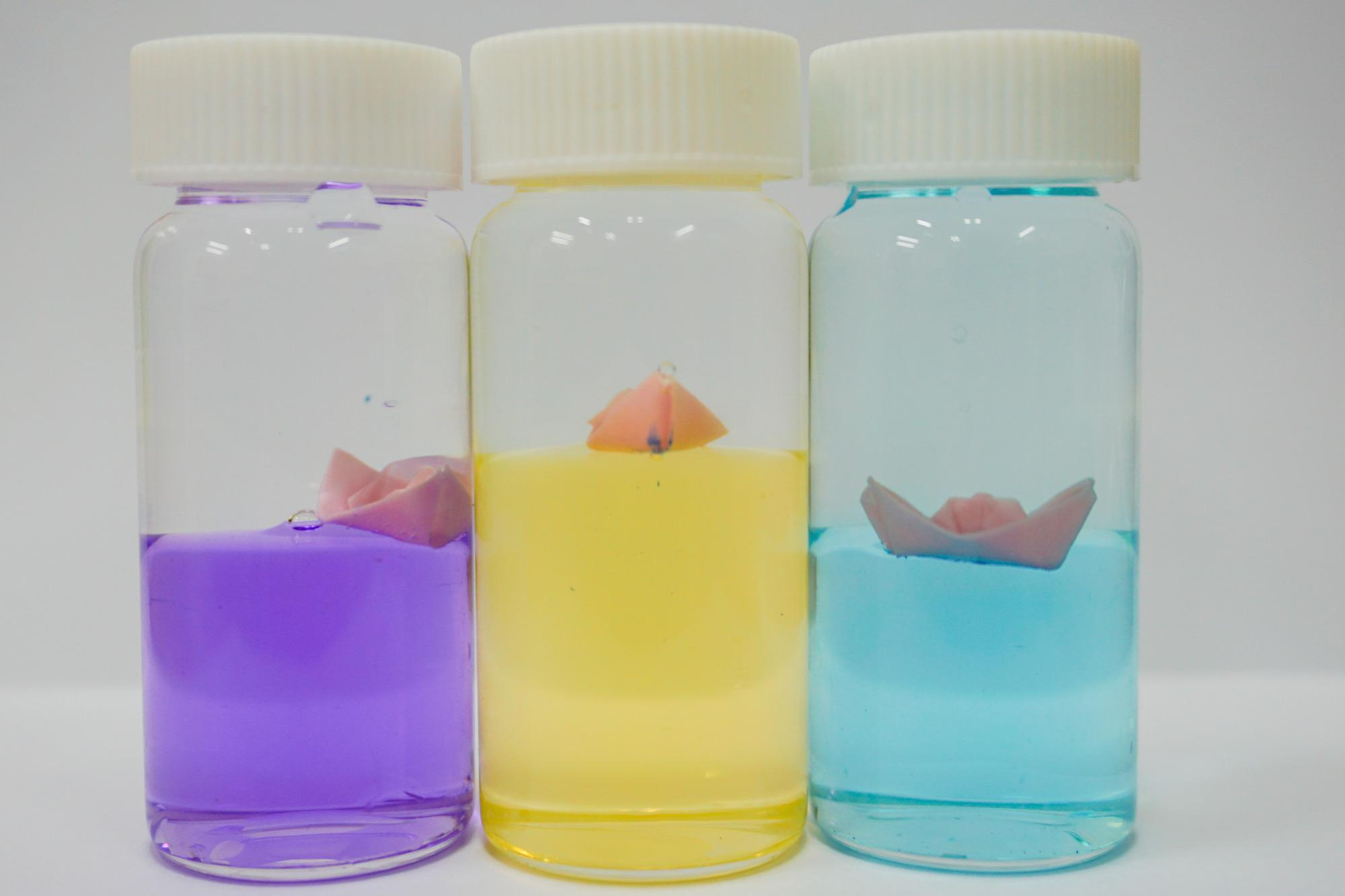
* 생각해보기
Q. 만들어진 종이배에 색칠을 하는 이유는 무엇일까요?
Q. 종이배가 물과 다이클로로메테인 사이에서 안정적으로 위치하는 이유는 무엇일까요?
심화Q.
다이클로로 메테인(CH2Cl2)은 쌍극자모멘트가 1.7D 정도의 큰 극성을 가진 물질이다.(물은 1.84D의 쌍극자 모멘트를 가진다.)
그럼에도 물과 잘 섞이지 않는데 그 이유는 무엇일까?
A.
두 액체가 섞이려면 두 액체의 친화도가 높아야 합니다. 다이클로로메테인의 쌍극자 모멘트는 1.7D 정도로 큰 극성을 가진 액체이지만, 물 분자와 상호작용할 수 있는 작용기를 가지고 있지 않습니다. 다이클로로메테인의 탄소와 염소는 모두 물 분자와 친화도가 높지않아 서로 섞이지 않습니다. 쌍극자 모멘트는 극성을 알 수 있는 지표이지만, 극성을 가진다고 하여 모든 극성물질이 잘 섞이는 것은 아닙니다.
'Chemistry' 카테고리의 다른 글
| 비타민C 정량 분석 실험 (0) | 2021.10.20 |
|---|---|
| 수질검사 실험 (18) | 2021.10.19 |
| 물의 경도 측정 실험 (0) | 2021.10.18 |
| 수돗물 속 염화 이온의 정량 분석 실험 (0) | 2021.10.14 |
| 시계반응 - 화학반응속도 실험 (0) | 2021.10.13 |



